La neuromodulación representa una estrategia terapéutica prometedora en la medicina moderna, que busca modificar la actividad del sistema nervioso mediante estímulos físicos, químicos o eléctricos dirigidos, con el fin de restaurar, regular o alterar las funciones neuronales. Se ha consolidado como alternativa o complemento a los tratamientos farmacológicos convencionales, especialmente en enfermedades neurológicas y psiquiátricas. A diferencia de los fármacos sistémicos, permite una intervención localizada, reversible y ajustable.
En los últimos años, la biotecnología ha potenciado esta disciplina al introducir dispositivos más inteligentes, miniaturizados y conectados. Esta sinergia permite desarrollar tratamientos más eficaces, seguros y personalizados.
En este contexto, la biotecnología ha comenzado a desempeñar un papel clave en el desarrollo de nuevas estrategias terapéuticas dirigidas al sistema nervioso, particularmente a través de la neuromodulación, una técnica que busca modificar la actividad neuronal mediante estímulos físicos, químicos o eléctricos. Esta disciplina, tradicionalmente vinculada a la neurocirugía y la ingeniería médica, ha encontrado en la biotecnología una aliada para avanzar hacia soluciones más precisas, adaptativas y menos invasivas.
Así, la neuromodulación biotecnológica representa una de las fronteras más prometedoras de la medicina de precisión. Esta disciplina se basa en la aplicación de dispositivos, biomoléculas o células modificadas para alterar, de forma específica y controlada, la actividad del sistema nervioso central o periférico. Su versatilidad permite abordar patologías neurológicas, psiquiátricas e incluso inmunológicas con una eficacia hasta ahora inalcanzable mediante terapias convencionales.
En este sentido, la neuromodulación biotecnológica integra avances como implantes inteligentes, nanodispositivos, sistemas de estimulación cerrada y algoritmos de aprendizaje automático, que permiten personalizar la terapia según la respuesta individual del paciente.
En este sentido, la estimulación cerebral profunda de circuito cerrado, como el sistema AlphaDBS desarrollado por Newronika, representa un gran paso al adaptar el estímulo en tiempo real a la actividad cerebral registrada. O el sistema Telepathy creado por Neuralink, que busca restaurar funciones cerebrales dañadas.
En el ámbito de las enfermedades neurodegenerativas, startups como Sinaptica Therapeutics han desarrollado plataformas como SinaptiStim®, basadas en neuromodulación no invasiva, que han mostrado en ensayos preliminares la capacidad de ralentizar el deterioro cognitivo en pacientes con Alzheimer.
Estas tecnologías emergentes también están siendo exploradas para condiciones como la migraña (Salvia BioElectronics) o la apnea del sueño (Nyxoah), con un creciente interés por parte de inversores y agencias reguladoras.
Por otro lado, la investigación básica continúa aportando nuevos conocimientos sobre los sistemas de neuromodulación natural del cerebro. El proyecto europeo StateNeuromod, financiado por el ERC, busca comprender cómo interactúan diferentes neuromoduladores como dopamina, serotonina y norepinefrina en la comunicación entre el hipocampo y la corteza prefrontal, lo cual podría guiar futuras terapias basadas en modelos de modulación multiquímica.
Al igual que los biomarcadores redefinieron el diagnóstico y pronóstico clínico, la neuromodulación biotecnológica redefine la forma en que concebimos la interacción con la red neuronal humana. En este contexto, tecnologías como la optogenética, la bioelectrónica inteligente o los biosensores celulares modificados, abren la puerta a tratamientos más personalizados, menos invasivos y con menores efectos secundarios.
A continuación, se presentan algunas de las principales tecnologías emergentes en neuromodulación (Tabla 1):
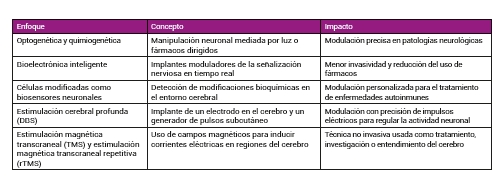
Sobre estas líneas, se presentan algunas de las principales tecnologías emergentes en neuromodulación.
Optogenética y quimiogenética: estas herramientas permiten controlar la actividad de poblaciones neuronales específicas mediante la introducción de proteínas sensibles a la luz (optogenética) o a fármacos diseñados (quimiogenética). Esto permite inducir o inhibir respuestas neuronales con una precisión milimétrica, revolucionando modelos experimentales de epilepsia, Parkinson o depresión resistente.
Bioelectrónica inteligente: los dispositivos implantables, como los estimuladores del nervio vago, ofrecen la posibilidad de modular la actividad del sistema nervioso autónomo en tiempo real.
Se han convertido en herramientas terapéuticas clave en epilepsia refractaria, depresión mayor y trastornos inflamatorios. Esta aproximación bioelectrónica busca reemplazar o complementar terapias farmacológicas prolongadas.
Células modificadas como biosensores neuronales: el uso de células modificadas genéticamente para detectar cambios bioquímicos en el entorno neuronal permite una retroalimentación continua de la actividad cerebral. Esto habilita sistemas terapéuticos adaptativos en enfermedades neurodegenerativas y autoinmunes, como la esclerosis múltiple.
Estimulación cerebral profunda (DBS): la técnica de neuromodulación más establecida, que implica la implantación quirúrgica de electrodos en áreas específicas del cerebro liberando impulsos eléctricos. Es ampliamente utilizada en el tratamiento de la enfermedad de Parkinson, el temblor esencial y la distonía. Los estudios actuales de esta técnica se centran en la capacidad de programar con precisión los estímulos y la miniaturización de los dispositivos.
Estimulación magnética transcraneal (TMS) y estimulación magnética transcraneal repetitiva (rTMS): estas técnicas no invasivas se basan en el uso de campos magnéticos para inducir corrientes eléctricas en zonas específicas del cerebro. Se utiliza para el tratamiento de la depresión mayor cuando los antidepresivos no han sido efectivos. También como herramienta diagnóstica y de investigación.
La regulación de estas tecnologías emergentes se encuentra en evolución, dada su naturaleza híbrida entre dispositivo médico, producto biotecnológico y, en algunos casos, terapia avanzada (como los ATMPs). En Europa, su desarrollo está guiado por la normativa del Reglamento (UE) 2017/745 sobre productos sanitarios (MDR), así como por el Reglamento (CE) n.º 1394/2007 sobre medicamentos de terapia avanzada.
La Agencia Europea del Medicamento (EMA) recomienda la evaluación caso por caso, especialmente cuando se utilizan vectores virales o modificaciones celulares. Asimismo, deben cumplirse estándares GMP y GLP en todos los procesos de fabricación y validación preclínica. En España, la AEMPS sigue estas directrices y ha comenzado a integrar comités ético-científicos para valorar su aplicabilidad clínica.
Uno de los temas de conflicto más notables en la neuromodulación biotecnológica gira en torno al neurocontrol y la privacidad mental. La posibilidad de intervenir con precisión sobre circuitos neuronales plantea dilemas bioéticos sobre la autonomía del paciente, el consentimiento informado y el riesgo de uso no terapéutico.
Otro debate se centra en la equidad en el acceso a estas tecnologías, que por su coste elevado tienden a concentrarse en centros de investigación o clínicas especializadas. Además, su validación científica, aunque prometedora, aún requiere consolidación en grandes cohortes clínicas, lo cual implica retos logísticos y regulatorios. La neuromodulación biotecnológica se perfila como una estrategia disruptiva en el abordaje terapéutico del sistema nervioso.
Su potencial para actuar de forma selectiva, dinámica y mínimamente invasiva la convierte en una herramienta fundamental de la medicina del futuro. Sin embargo, es crucial establecer marcos éticos, regulatorios y científicos robustos que aseguren su desarrollo seguro y equitativo.
La integración de estas tecnologías en el arsenal clínico permitirá reducir la carga farmacológica en pacientes crónicos, mejorar la calidad de vida y fomentar el diseño de tratamientos personalizados según el patrón de activación neuronal de cada individuo.
Bibliografía
- Adams, Z. H., Hart, E. C., & Patel, N. K. (2025). Deep brain stimulation for control of refractory hypertension. Autonomic neuroscience : basic & clinical, 260, 103286. https://doi.org/10.1016/j.autneu.2025.103286
- Birmingham, K., Gradinaru, V., Anikeeva, P., Grill, W. M., Pikov, V., McLaughlin, B., Pasricha, P., Weber, D., Ludwig, K., & Famm, K. (2014). Bioelectronic medicines: A research roadmap. Nature Reviews Drug Discovery, 13(6), 399–400. https://doi.org/10.1038/nrd4351
- European Medicines Agency. (2022). Guideline on quality, non-clinical and clinical requirements for medical devices. EMA/CHMP/QWP/245074/2015
- Famm, K., Litt, B., Tracey, K. J., Boyden, E. S., & Slaoui, M. (2013). A jump-start for electroceuticals. Nature, 496(7444), 159–161. https://doi.org/10.1038/496159a
- Guggenmos, D. J., Rao, S., & McIntyre, C. C. (2023). Modeling multineurotransmitter modulation in prefrontal–hippocampal circuits. Frontiers in Neuroscience, 17, 1156. https://doi.org/10.3389/fnins.2023.01156
- Laviña, B., De Greef, B., & Reardon, S. (2022). The rise of neuromodulation startups in Europe. Labiotech.eu.
- Ministerio de Sanidad. (2023). Estrategia en enfermedades neurológicas y crónicas complejas. Consejo Interterritorial del SNS.
- Peña-Ortega, F. (2019). Optogenética y quimiogenética: herramientas para estudiar la actividad cerebral y el comportamiento. Revista Mexicana de Neurociencia, 20(2), 45–54.
- Priori, A., Foffani, G., Rossi, L., & Marceglia, S. (2020). Adaptive deep brain stimulation (aDBS) controlled by local field potential oscillations. Experimental Neurology, 323, 113074. https://doi.org/10.1016/j.expneurol.2019.113074
- Sinaptica Therapeutics. (2024). SinaptiStim® Clinical Overview. https://sinapticatx.com
Descarga sugerida:
Artículo escrito por:
Álvaro Alonso Carrero, Ismael Pérez Carrobles y Javier Raboso Gallego
Alumno, Preclínica Regulatoria y Preclínica Regulatoria, respectivamente
Konexio Biotech



