Desde la publicación del Anexo 1 de fabricación de estériles, las plantas farmacéuticas han hecho un esfuerzo importante por revisar sus instalaciones y procesos para adecuarse a los nuevos requerimientos. En algunos casos, esto ha supuesto sólo ajustes menores, pero en otros, los cambios han sido estructurales y han impactado directamente en la forma de operar.
Durante esta fase inicial, la prioridad de muchas organizaciones ha sido garantizar el cumplimiento normativo y recuperar la operatividad lo antes posible. Sin embargo, una vez implantadas las medidas y con cierta experiencia acumulada sobre las nuevas dificultades, es momento de dar un paso más allá. Tal y como propone la Estrategia de Control de Contaminación (CCS), entendida como una herramienta de conocimiento integral del proceso y de mejora continua, este es el momento de revisar con otra mirada: ¿cómo podemos hacer que nuestros procesos sean más eficientes?
Este artículo plantea algunas consideraciones para revisar y optimizar procesos clave en el control de la contaminación. Procesos que, además de ser imprescindibles para el cumplimiento, tienen un gran impacto en los costes operativos, el consumo de recursos y la sostenibilidad.
Uno de los pilares del control de la contaminación es la Limpieza y Desinfección en salas blancas. Su impacto sobre el control microbiológico es indiscutible, pero también lo es sobre los recursos que consume: productos, tiempo y personal.
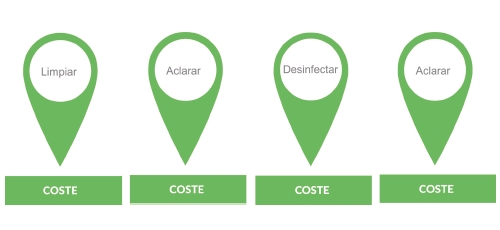
Según las recomendaciones del Anexo 1, este proceso debería contemplar no solo la limpieza y desinfección, sino también la gestión de residuos. Un planteamiento estándar, considerando el cumplimiento, puede incluir hasta cuatro etapas: limpieza, aclarado, desinfección y nuevo aclarado. Sin embargo, si vamos más allá y revisamos el proceso desde el punto de vista de la eficiencia, nos planteamos: ¿podemos reducir los aclarados según el tipo de agente de desinfección? Y según esto, ¿es viable espaciar los intervalos entre limpiezas sin comprometer el control microbiológico?
Considerar factores como los compuestos químicos empleados, los materiales de los útiles, los regímenes de aplicación y los métodos puede marcar la diferencia entre un proceso simplemente conforme y uno realmente optimizado. Existen escenarios donde dos procesos igualmente válidos desde el punto de vista normativo pueden tener un impacto muy distinto en coste y productividad.
Otro punto clave es el lavado de materiales reutilizables en salas blancas. Aquí, el uso del modelo del Círculo de Sinner, que relaciona temperatura, acción mecánica, química (detergente) y tiempo, permite evaluar objetivamente los factores que influyen en la eficacia del proceso.
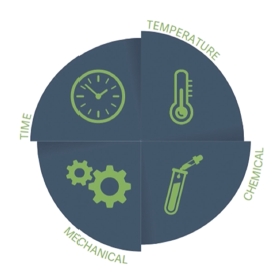
¿Puede un lavado automático optimizar recursos respecto a uno manual? ¿Qué tipo de piezas estamos manipulando? Evaluar el proceso, los 4 factores que influyen en el proceso y el equipo que podríamos utilizar permite tomar decisiones informadas para rediseñar ciclos más eficientes.
La mejora de este proceso no es solo una cuestión de cumplimiento, sino una oportunidad para reducir costes, tiempos de inactividad, evitar repetir trabajos y liberar recursos operativos.
La gestión eficaz de los equipos de acero inoxidable en la industria farmacéutica no puede limitarse a la inspección visual o al mantenimiento correctivo. Fenómenos como el rouging —la formación de óxidos de hierro en la superficie interna de sistemas de agua para inyectables (WFI), vapor puro (PS) y depósitos de almacenamiento— representan un desafío creciente. Estos depósitos, además de comprometer la integridad del material y la calidad del producto, pueden derivar en desviaciones críticas durante auditorías y generar altos costes de mantenimiento.
Tradicionalmente, los procesos de derouging se han apoyado en soluciones ácidas fuertes o suaves, cuya efectividad es conocida, pero que presentan limitaciones importantes: riesgo de ataque químico al cromo y níquel, generación de residuos peligrosos y necesidad de neutralización del agua de aclarado. Por este motivo, la industria está avanzando hacia soluciones de limpieza y pasivación basadas en productos de pH neutro, que permiten una intervención más segura, sostenible y eficaz.
Este enfoque de cuatro etapas (limpieza inicial, derouging, pasivación y aclarado final) utiliza productos químicos que eliminan selectivamente los óxidos de hierro sin afectar la capa pasiva del acero inoxidable y, a continuación, una solución específica restaura dicha capa, rica en óxido de cromo, devolviendo al material su resistencia original a la corrosión. El proceso, validado en sistemas críticos, reduce tiempos de parada, elimina la necesidad de neutralización de efluentes y minimiza riesgos para el personal operativo, lo que también conlleva un gran ahorro económico.
El resultado es un método compatible con los principios de la mejora continua en la Estrategia de Control de la Contaminación (CCS): más eficiente, respetuoso con el medio ambiente y alineado con las exigencias regulatorias (GMP y ASTM A967). Además, al tratarse de un procedimiento adaptable, puede aplicarse tanto en circuitos de agua ultrapura como en equipos de proceso (reactores, tanques, autoclaves) sin comprometer la operatividad de la planta.
Sin embargo, el cambio estructural que ha supuesto más impacto en las plantas farmacéuticas es la recomendación del Anexo I al uso de sistemas de barreras para proteger la fabricación del producto estéril de los operarios, y con ello, el reto de realizar de nuevo los mismos procesos teniendo en cuenta la barrera física de un Rabs o aislador.
Como se indicaba al inicio, el objetivo inicial era recuperar la operatividad lo antes posible. Pero ahora, con una nueva perspectiva, es el momento de plantear mejoras en aspectos clave como el uso y control de los guantes, el material más crítico en muchos procesos, y el proceso de transferencia de materiales, uno de los puntos más sensibles en términos de riesgo de contaminación en la zona de fabricación.
Los guantes son la barrera física entre el operario y el interior del sistema de barrera, lo que explica su papel fundamental. El primer punto indispensable para una gestión eficaz comienza por una correcta selección: no todos los guantes son adecuados para todos los procesos, ni para todos los usuarios.
Elegir el modelo correcto permite evitar roturas, desgaste prematuro y pérdida de ergonomía, factores que acortan su vida útil y aumentan la dificultad en las operaciones rutinarias. Todo ello conlleva una posible pérdida de eficacia y un mayor riesgo de desviación.
En la elección del guante deben tenerse en cuenta elementos como el tipo y tamaño de puerto, la longitud y talla del guante, la talla de mano del usuario y, por supuesto, el material y espesor. Este último factor es determinante para garantizar su compatibilidad con los métodos de descontaminación o esterilización que se emplean en rutina. Esta decisión también influirá directamente en la gestión de cambios, las tareas de mantenimiento y la durabilidad del sistema de guantes.
Por otro lado, si revisamos los procesos de transferencia de materiales, también aquí hay margen para la eficiencia. Es fundamental estudiar cada tipo de material y su circunstancia específica: ¿llega ya esterilizado? ¿se introduce por autoclave? ¿el destino del material es el interior de un aislador? ¿se va a descontaminar con la carga o lo introduciremos en la rutina de fabricación?
Cada casuística tiene condicionantes propios, y solo analizando cada una por separado podremos aplicar el proceso más adecuado para optimizar tiempos, recursos y minimizar riesgos. Para ello, conviene considerar:
- El programa de biodescontaminación asociado
- El alcance de la automatización disponible
- El impacto de la manipulación sobre el sistema de guantes
- Los mecanismos de transferencia utilizados (puertos, RTP, liners, etc.)
- Y el riesgo potencial asociado a la pérdida de integridad de la barrera o del guante
Este análisis estructurado no solo permite estandarizar procesos de transferencia, sino también reducir intervenciones manuales, mejorar la trazabilidad y reforzar la robustez global del sistema de contención.
En el control de la contaminación, uno de los procesos más críticos es la obtención y gestión de los datos de monitorización. Tener un sistema eficaz no solo permite mejorar el propio proceso, sino también acceder a los datos de forma más ágil, evaluarlos con precisión y disponer de una visión global de lo que ocurre en planta. Esta es, sin duda, la base para impulsar una verdadera mejora continua.
Integrar la monitorización ambiental en todos los niveles del proceso, digitalizarla y automatizarla es clave para optimizar recursos. Esto permite reducir costes, minimizar riesgos de contaminación, mejorar la eficacia de los muestreos y avanzar hacia una operativa más sostenible. Pero, sobre todo, mejora la fiabilidad de la información y con ello la calidad de la toma de decisiones.
También es importante tener en cuenta factores operativos que, aunque parecen menores, marcan la diferencia. Elegir medios de cultivo con caducidades largas reduce ensayos innecesarios en la recepción; optar por placas con mayor volumen de medio evita su desecación durante la exposición y mejora la viabilidad de los microorganismos; o seleccionar formatos que no requieran refrigeración ayuda a reducir el consumo energético. Asimismo, disponer de equipos adecuados, para viables y no viables, que minimicen las intervenciones y el impacto sobre el flujo laminar mejora la fiabilidad de los datos y contribuye a procesos más sostenibles.
Y si queremos ir más allá, las soluciones de microbiología rápida representan sin duda una evolución clave para los laboratorios. Reducir los días necesarios para obtener resultados, o incluso disponer de una monitorización en continuo, puede marcar una diferencia crítica en la capacidad de anticiparse y actuar. Es ahí donde reside gran parte del potencial para hacer los procesos más eficientes.
Por tanto, revisar y optimizar los procesos de control de la contaminación no es sólo una exigencia regulatoria: es una decisión estratégica.
La CCS no es un fin en sí misma, sino un marco de trabajo para revisar de forma crítica los procesos que afectan al control de la contaminación. Una vez superada la primera etapa de cumplimiento, se abre una oportunidad clave para optimizar lo que ya existe.
Aplicar la filosofía de la mejora continua permite a las empresas reducir costes, aumentar su eficiencia operativa y garantizar un cumplimiento sólido, todo ello sin comprometer la seguridad del paciente ni la calidad del producto.
Revisar las rutinas de limpieza, redefinir los criterios del lavado de materiales o digitalizar la monitorización ambiental son acciones que, desde una visión integral, permiten ganar en eficiencia, reducir costes operativos y reforzar la capacidad de respuesta ante desviaciones o inspecciones.
Y sobre todo, permiten construir un sistema más robusto, más sostenible y alineado con los principios de mejora continua que toda estrategia de control debe aspirar a incorporar de forma viva en la planta.
Descarga sugerida:
Artículo escrito por:
Tiselab