Más que ninguna otra metodología, la microscopía electrónica ha contribuido a nuestro conocimiento de la organización de las células y de la estructura de los virus. La microscopía electrónica sigue jugando un papel clave en el descubrimiento de nuevos organismos, sobre todo virus y es de gran ayuda para estudiar las etapas de su ciclo vital. Cualquiera de esas etapas es susceptible de ser bloqueada por un fármaco antiviral. Y para validar y comprender el mecanismo de acción de los antivirales, la microscopía electrónica está jugando un importante papel.
Si bien la pandemia causada por el coronavirus SARS-CoV-2 ha puesto de manifiesto que contamos con muy pocas medicinas para tratar las infecciones virales, actualmente existen numerosas investigaciones para conseguir colecciones de fármacos antivirales eficaces y de amplio espectro, es decir, compuestos que puedan tratar las infecciones causadas por virus diferentes. Por poner solo un ejemplo, actualmente hay 509 ensayos clínicos registrados en www.clinicaltrials.gov para validar compuestos con actividad antiviral contra los coronavirus (revisado el 22 de marzo de 2024). De ellos, 66 están en fase inicial, 24 están activos, 210 completados y 58 terminados.
¿Qué virus se consideran importantes actualmente? La Organización Mundial de la Salud tiene una lista de las diez enfermedades prioritarias para las que se necesitan tratamientos urgentes1. En ella se recogen las enfermedades causadas por coronavirus, bunyavirus, filovirus, paramixovirus y el flavivirus Zika. La lista incluye también la “Enfermedad X” y se refiere a la que podría causar un patógeno aún desconocido para el que deberíamos estar preparados. En este contexto lo ideal sería contar con una colección de fármacos antivirales de amplio espectro que fueran eficaces contra los virus conocidos y los que están por venir.
Un antiviral es una molécula que bloquea una etapa concreta del ciclo vital de un virus. Los antivirales son básicamente de dos tipos: 1) antivirales de acción directa, que atacan componentes de los virus y 2) antivirales que atacan componentes de las células que los virus necesitan para infectar. Una importante fuente para nuevos antivirales viene de lo que se conoce como reposicionamiento de fármacos2. Cruzando información acerca de lo que los virus usan en las células y lo que los fármacos bloquean en las células se están encontrando compuestos ya usados en clínica para tratar diversas enfermedades y que pueden reposicionarse para tratar las infecciones virales.
Para estudiar la capacidad antiviral de un compuesto, se aplican técnicas de virología y bioquímica. Si además se aplican técnicas de microscopía óptica y electrónica, la caracterización del nuevo compuesto será mucho más completa3. La microscopía óptica de células vivas nos permite estudiar las infecciones virales de manera dinámica y a tiempo real. Por otro lado, los virus son pequeños y dado que su tamaño va de unos pocos nanómetros a aproximadamente una micra, sólo pueden verse con detalle con la resolución que proporciona el microscopio electrónico, que consigue una magnificación y resolución espacial de más de mil veces superior a la que proporcionan los microscopios ópticos4. La microscopía electrónica nos da detalles de cómo los virus entran en las células, cómo construyen las factorías donde replican su genoma y donde ensamblan los nuevos virus infecciosos y cómo salen de las células. Gracias a los avances técnicos en microscopía, estamos empezando a ser conscientes de la variedad y complejidad de las estructuras que los virus construyen dentro de las células5. Y cómo se ven afectadas por la acción de los antivirales.
La primera figura de este artículo (creada con BioRender.com) resume la estrategia general a seguir para estudiar el efecto de los antivirales con técnicas de imagen. La microscopía óptica nos permite estudiar los efectos del antiviral en la progresión de la infección, bien usando virus fluorescentes o marcando componentes virales con anticuerpos específicos y fluoróforos mediante las técnicas de inmunofluorescencia. Así podemos saber de forma rápida en cuántas células no hay señal del virus, lo que significa que la infección ha sido bloqueada por el antiviral. Si disponemos de virus fluorescentes con las técnicas de video-microscopía de células vivas podemos analizar los cambios en la progresión de la infección a tiempo real. Para visualizar las infecciones con detalle, acudimos a la microscopía electrónica convencional, que conlleva el procesamiento y estudio de las muestras a temperatura ambiente. Son técnicas rápidas que permiten dar un resultado en pocos días. Si se quiere hacer un estudio a mayor resolución, se acude a la microscopía electrónica a baja temperatura o “criomicroscopía electrónica”. Son métodos que preservan el material biológico en un estado próximo al nativo y cuya aplicación requiere más tiempo, por lo que se aplican para estudiar detalles concretos. El carácter dinámico de la microscopía óptica puede combinarse con el detalle y resolución de la microscopía electrónica gracias la microscopía correlativa. Estas técnicas nos permiten seleccionar células con un patrón interesante en el microscopio óptico y estudiarlas en el microscopio electrónico6. Así podemos estudiar qué sucede dentro de las células en las que el fármaco antiviral tiene éxito y también en las que el virus no es bloqueado por el antiviral y por tanto obtener datos sobre cómo aparece en las células la resistencia a los antivirales7.
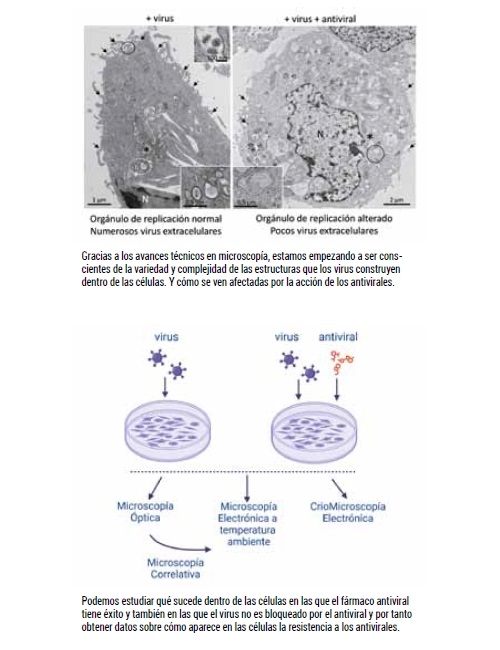
En la segunda figura podemos ver un ejemplo del tipo de información que nos proporciona la microscopía electrónica convencional. Se trata de células Vero infectadas con SARS-CoV-2, el coronavirus causante de la Covid-19, tratadas sin y con un compuesto antiviral, la hidroxipropil-β-ciclodextrina (HβCD). Las células infectadas presentan grupos de vesículas de doble membrana (asteriscos) que constituyen el orgánulo de replicación del virus, así como numerosos virus extracelulares (flechas). Cuando son tratadas con HβCD, el orgánulo de replicación está alterado y sus vesículas de doble membrana aparecen deformes y vacías8. También se observan menos virus extracelulares.
Otros ejemplos son:
1) la plitidepsina, compuesto antitumoral que inhibe la infección del SARS-CoV-2 y que también tiene como diana el orgánulo de replicación del virus, que no llega ni a formarse en presencia del compuesto. La microscopía electrónica mostró que tampoco se forman partículas virales9.
2) El ácido acetil salicílico, una de las medicinas más usadas en el mundo para tratar el dolor y la inflamación, inhibe la infección del virus Bunyamwera, el prototipo del orden Bunyavirales. Este grupo de virus incluye patógenos importantes para humanos, animales y plantas. La microscopía electrónica mostró que el ácido acetil salicílico altera el aparato de Golgi, que es el orgánulo en el que el virus establece sus complejos replicativos para copiar su genoma. Y lo hace de manera reversible porque al retirar el fármaco, el aparato de Golgi de las células recupera su morfología normal10. Este ejemplo nos muestra que la microscopía electrónica nos permite estudiar los efectos secundarios de los antivirales en las células y también si son reversibles una vez que se retira el fármaco.
3) La digoxina, compuesto que se utiliza para tratar enfermedades cardíacas, también inhibe la infección de bunyavirus. La microscopía electrónica mostró que la digoxina no altera el aparato de Golgi sino las mitocondrias, que el virus utiliza como uno de los componentes de sus factorías de replicación11.
4) Las nanopartículas de plata tienen acción antimicrobiana y también bloquean la infección de bunyavirus. La microscopía electrónica reveló que se unen a la superficie del virus dificultando su unión a las células6.
5) La microscopía electrónica mostró que en neuronas el compuesto rottlerina bloquea el transporte intracelular del bunyavirus La Crosse en el aparato de Golgi, por lo que los virus quedan atrapados dentro de las células y no pueden propagarse a las células vecinas. Este compuesto también inhibe la encefalitis que el virus causa en ratones12.
6) El compuesto SBI-0090799 bloquea la formación del compartimento membranoso de replicación del virus Zika13.
7) el compuesto C19orf66 tiene un mecanismo de acción similar en células infectadas por el virus de la hepatitis C7.
Los virus emergentes y re-emergentes son una amenaza para la salud pública y necesitamos tratamientos eficaces para combatirlos. La microscopía electrónica nos asiste en el diagnóstico, en la identificación de los efectos secundarios de los fármacos, en la caracterización de los mecanismos de acción de los antivirales y en la comprensión de por qué a veces fallan.
Agradecimientos
La autora quiere expresar su gratitud a los colaboradores, Dr. Martin Sachse (Instituto de Salud Carlos III), Dr. Moisés García Serradilla y Dra Beatriz Pacheco (Universidad Complutense de Madrid), Dr. José P. Cerón (CUD, Universidad Politécnica de Cartagena) y a los miembros actuales y antiguos del Laboratorio de Estructura Celular del Centro Nacional de Biotecnología (CNB-CSIC), Dra Isabel Fernández de Castro Martín, Dra Raquel Tenorio Vela, Dña Sara Yolanda Fernández Sánchez, Dr. Alberto Fernández Oliva y Dra Paula Ortega González, por su participación en los trabajos citados en este artículo.
Bibliografía
- https://www.who.int/activities/prioritizing-diseases-for-research-and-development-in-emergency-contexts (revisada el 26 de marzo de 2024).
- García-Serradilla M et al. (2019) Drug repurposing for new, efficient, broad spectrum antivirals. Virus Res 264:22-31.
- Risco C (2021) Application of advanced imaging to the study of virus-host interactions. Viruses 13(10):1958. doi: 10.3390/v13101958.
- Bozzola JJ y Russell LD (1998) Electron Microscopy: Principles and Techniques for Biologists (2nd ed.) Jones and Bartlett Publishers, Inc.
- Sachse M et al. (2019) The viral replication organelles within cells studied by electron microscopy. Adv. Virus Res. 105:1-33. doi: 10.1016/bs.aivir.2019.07.005.
- García-Serradilla M y Risco C (2021) Light and electron microscopy imaging unveils new aspects of the antiviral capacity of silver nanoparticles in bunyavirus-infected cells. Virus. Res. 302:198444. doi: 10.1016/j.virusres.2021.198444.
- Kinast et al. (2020) C19orf66 is an interferon-induced inhibitor of HCV replication that restricts formation of the viral replication organelle. J. Hepatol. 73:549-558.
- Raïch-Regué D et al. (2023) β-Cyclodextrins as affordable antivirals to treat coronavirus infections. Biomed. Pharmacother. 164:114997. doi: 10.1016/j.biopha.2023.114997.
- Sachse M et al. (2022) Unraveling the antiviral activity of plitidepsin against SARS-CoV-2 by subcellular and morphological analysis. Antiviral Res. 200:105270. doi: 10.1016/j.antiviral.2022.105270.
- Fernández-Sánchez SY et al. (2023) Antiviral activity of acetylsalicylic acid against Bunyamwera virus in cell culture. Viruses 15(4):948. doi: 10.3390/v15040948.
- Pacheco B et al. (2023) Digoxin is a potent inhibitor of Bunyamwera virus infection in cell culture. J. Gen. Virol. 104(4). Doi: 10.1099/jgv.0.001838.
- Ojha D et al. (2021) Rottlerin inhibits La Crosse virus-induced encephalitis in mice and blocks release of replicating virus from the Golgi body in neurons. Nat Microbiol. 6:1398-1409.
- Riva et al. (2021) The compound SBI-0090799 inhibits Zika virus infection by blocking de novo formation of the membranous replication compartment. J. Virol. 95:e00996-21.
Descarga sugerida:
Artículo escrito por:
Cristina Risco Ortiz
Investigadora Científica
CSIC en el Centro Nacional de Biotecnología, Madrid