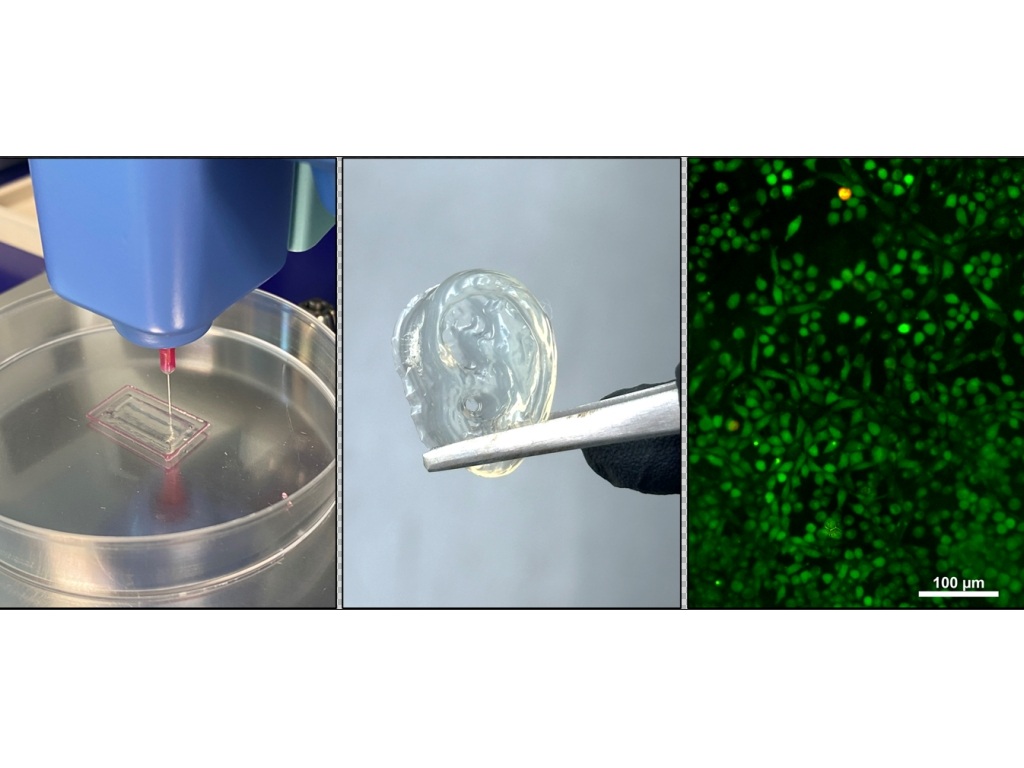
La impresión 3D de hidrogeles se ha consolidado en los últimos años como una de las herramientas más versátiles dentro de la biofabricación y la ingeniería de tejidos. Frente a otros métodos de conformado de biomateriales, permite generar estructuras tridimensionales con control geométrico, arquitecturas internas definidas y propiedades mecánicas ajustables. Estas capacidades han impulsado su uso tanto en el desarrollo de modelos biológicos in vitro como en la fabricación de andamios funcionales y dispositivos médicos avanzados 1–4.
Dentro de este campo, los sistemas fotocurables —hidrogeles que reticulan o curan tras la exposición a la luz— han adquirido un protagonismo creciente debido a su flexibilidad de procesado y a su potencial para desacoplar el momento de deposición del de estabilización estructural 5,6. Las tintas fotocurables se caracterizan porque pueden extruirse en estado fluido y fijar posteriormente su estructura mediante iluminación controlada, lo que permite mantener una viscosidad adecuada durante la impresión y, al mismo tiempo, alcanzar una red polimérica estable tras el curado. Sin embargo, su rendimiento no depende únicamente de la capacidad de reticular bajo luz. La ventana real de uso está determinada por el equilibrio entre comportamiento reológico, cinética de polimerización, estabilidad dimensional y compatibilidad celular 7. De hecho, en la práctica, muchas formulaciones que funcionan correctamente desde el punto de vista mecánico o de impresión fallan cuando se evalúan biológicamente, mientras que otras muy biocompatibles presentan problemas de fidelidad estructural. Por esta razón, el desarrollo de hidrogeles fotocurables exige un enfoque integrado que combine ciencia de materiales, reología y validación biológica.
Imprimibilidad: más allá de la viscosidad
Desde el punto de vista del procesado, la reología suele ser el primer filtro que determina si una formulación es realmente imprimible 8,9. En sistemas de extrusión, el material experimenta tasas de cizalla elevadas en el interior de la boquilla y condiciones de bajo esfuerzo una vez depositado. Para que el proceso sea estable, la tinta debe presentar un comportamiento no newtoniano con adelgazamiento por cizalla, de modo que fluya con facilidad durante la impresión y recupere parcialmente su viscosidad tras la deposición.
Uno de los errores más habituales en este punto es evaluar la imprimibilidad únicamente a partir de la medida de viscosidad en un único punto. En realidad, el análisis de las curvas completas de flujo en función de la tasa de cizalla y su ajuste a modelos matemáticos permiten comparar formulaciones y anticipar su comportamiento en condiciones reales de proceso 10. Asimismo, los ensayos de recuperación estructural tras ciclos de cizalla aportan información sobre la capacidad del material para reconstruir parcialmente su red interna después de ser sometido a esfuerzos, algo directamente relacionado con la estabilidad de las capas impresas.
Formulación: equilibrio entre control estructural y bioactividad
Las formulaciones actuales de tintas fotocurables combinan con frecuencia polímeros sintéticos y componentes biológicos 10,11. Derivados acrilados de gelatina o polietilenglicol permiten ajustar la densidad de red y, por tanto, las propiedades mecánicas finales, mientras que proteínas como el colágeno introducen motivos bioactivos que favorecen la adhesión y la interacción celular.
Por otro lado, otro elemento crítico de la formulación es el sistema fotoiniciador, responsable de generar las especies reactivas que desencadenan la reticulación bajo iluminación 12. Aunque tradicionalmente se han empleado iniciadores activables en el rango UV, existe una tendencia clara hacia sistemas sensibles a longitudes de onda más altas, en la región violeta-azul, que resultan menos agresivas para las células. Entre ellos, el iniciador LAP ha ganado popularidad por su buena solubilidad en agua y su activación eficiente alrededor de 405 nm 13. No obstante, su concentración debe optimizarse cuidadosamente. Aumentar la cantidad de fotoiniciador puede acelerar la reticulación, pero también incrementar la presencia de fracciones residuales no reaccionadas si la conversión no es completa. Estas fracciones residuales pueden tener un impacto directo sobre la viabilidad celular, por lo que el equilibrio entre eficacia de reticulación y citocompatibilidad es esencial 7,14,15.
Procesado y curado: modular las propiedades sin cambiar la formulación
Una de las grandes ventajas de los sistemas fotocurables es que las propiedades mecánicas finales no dependen exclusivamente de la composición química. Parámetros de proceso como la intensidad de la luz, el tiempo de exposición o la geometría de iluminación influyen directamente en la densidad de reticulación alcanzada. Esto permite modular la rigidez del hidrogel tras la impresión sin modificar la formulación de partida 7.
Dado que la respuesta celular es altamente sensible a la rigidez del entorno, esta capacidad de ajuste resulta especialmente valiosa en ingeniería de tejidos y en el diseño de modelos celulares. En este punto, los ensayos mecánicos no destructivos en tiempo real permiten seguir la evolución del módulo elástico durante la fotoreticulación y establecer correlaciones entre condiciones de curado y propiedades finales del material.
Compuestos extractables y acondicionamiento: una etapa crítica
Un aspecto que con frecuencia se subestima en los hidrogeles fotocurables es la presencia de compuestos extractables tras el curado. Fracciones de monómero no reaccionado, fotoiniciador libre o subproductos de reacción pueden quedar retenidos en la red y difundirse posteriormente al medio de cultivo 7. Aunque normalmente estas fracciones se encuentran en concentraciones bajas, su impacto biológico puede ser significativo, especialmente en cultivos celulares sensibles.
Por este motivo, los protocolos de lavado y acondicionamiento posteriores a la impresión no deben considerarse un paso accesorio, sino una fase esencial del proceso para garantizar la seguridad y el comportamiento biológico del material. En la práctica, periodos de lavado del orden de uno o dos días suelen ser suficientes para reducir de forma notable la fracción móvil. Así, la evaluación de la citocompatibilidad de estructuras impresas debería realizarse siempre sobre muestras previamente acondicionadas, ya que evaluar materiales recién curados puede llevar a conclusiones erróneas, atribuyendo al hidrogel una citotoxicidad intrínseca que en realidad está asociada a compuestos residuales transitorios.
Integridad estructural: evaluación del hinchamiento y la estabilidad del hidrogel
El comportamiento de hinchamiento aporta información complementaria sobre la integridad de la red polimérica. Una absorción de agua controlada y reproducible suele indicar estabilidad estructural, mientras que hinchamientos excesivos o muy variables pueden comprometer la fidelidad geométrica de la pieza impresa 16–18. El perfil temporal de hinchamiento suele reflejar tanto la capacidad de absorción como los procesos de relajación de la red, y se relaciona estrechamente con la difusión de compuestos residuales. Por ello, su evaluación complementa de forma natural los estudios de extractables y de estabilidad mecánica.
Hacia la búsqueda de caracterizaciones más completas
A medida que la bioimpresión avanza hacia aplicaciones más cercanas a producto y a entornos regulados, se hace cada vez más evidente la necesidad de caracterizaciones integrales y comparables entre materiales. No basta con demostrar que una tinta puede imprimirse: es necesario entender cómo fluye, cómo reticula, qué libera al medio, cómo se comporta en condiciones acuosas y cómo responden las células en contacto con ella.
El uso de componentes comerciales bien definidos, junto con metodologías de caracterización reproducibles, puede facilitar la transferencia de conocimiento entre grupos de investigación y entornos industriales. En biofabricación con sistemas fotocurables, la calidad del resultado final no depende únicamente de la impresora o del diseño digital, sino, en gran medida, de cómo se formula, se procesa y se caracteriza el material.
Referencias
- 1. Huang, G. et al. Applications, advancements, and challenges of 3D bioprinting in organ transplantation. Biomater. Sci. 12, 1425–1448 (2024).
- 2. de Vries, R. B. M. et al. The potential of tissue engineering for developing alternatives to animal experiments: a systematic review. J. Tissue Eng. Regen. Med. 9, 771–778 (2015).
- 3. Qiu, C. et al. A 3D‐Printed Dual Driving Forces Scaffold with Self‐Promoted Cell Absorption for Spinal Cord Injury Repair. Adv. Sci. 10, 1–16 (2023).ç
- 4. Jamróz, W., Szafraniec, J., Kurek, M. & Jachowicz, R. 3D Printing in Pharmaceutical and Medical Applications – Recent Achievements and Challenges. Pharm. Res. 35, (2018).ç
- 5. Lai, Y. et al. Photocrosslinkable Biomaterials for 3D Bioprinting: Mechanisms, Recent Advances, and Future Prospects. Int. J. Mol. Sci. 25, 12567 (2024).
- 6. Van Hoorick, J. et al. (Photo-)crosslinkable gelatin derivatives for biofabrication applications. Acta Biomater. 97, 46–73 (2019).
- 7. Morató-Cecchini, C. et al. Comprehensive Characterisation of Photocurable PEGDA/Gelatine Hydrogels for Extrusion-Based 3D Printing. Gels 12, 137 (2026).
- 8. Herrada-Manchón, H., Fernández, M. A. & Aguilar, E. Essential Guide to Hydrogel Rheology in Extrusion 3D Printing: How to Measure It and Why It Matters? Gels 9, 517 (2023).
- 9. Schwab, A. et al. Printability and Shape Fidelity of Bioinks in 3D Bioprinting. Chem. Rev. 120, 11028–11055 (2020).
- 10. Khoeini, R. et al. Natural and Synthetic Bioinks for 3D Bioprinting. Adv. NanoBiomed Res. 1, 2000097 (2021).
- 11. Babiak, P. M. et al. Tunable Blended Collagen I/II and Collagen I/III Hydrogels as Tissue Mimics. Macromol. Biosci. 24, 2400280 (2024).
- 12. Lim, K. S. et al. Fundamentals and Applications of Photo-Cross-Linking in Bioprinting. Chem. Rev. 120, 10662–10694 (2020).
- 13. Elkhoury, K., Zuazola, J. & Vijayavenkataraman, S. Bioprinting the future using light: A review on photocrosslinking reactions, photoreactive groups, and photoinitiators. SLAS Technol. 28, 142–151 (2023).
- 14. Lambrecht, S., Gazizova, A., Kara, S., Meyer, J. & Jopp, S. Antimicrobial properties and biocompatibility of semi-synthetic carbohydrate-based ionic hydrogels. RSC Adv. 14, 30719–30731 (2024).
- 15. Nguyen, A. K., Goering, P. L., Elespuru, R. K., Sarkar Das, S. & Narayan, R. J. The Photoinitiator Lithium Phenyl (2,4,6-Trimethylbenzoyl) Phosphinate with Exposure to 405 nm Light Is Cytotoxic to Mammalian Cells but Not Mutagenic in Bacterial Reverse Mutation Assays. Polymers (Basel). 12, 1489 (2020).
- 16. Lascombes, C. et al. Starch-carrageenan interactions in aqueous media: Role of each polysaccharide chemical and macromolecular characteristics. Food Hydrocoll. 66, 176–189 (2017).
- 17. Holback, H., Yeo, Y. & Park, K. Hydrogel swelling behavior and its biomedical applications. in Biomedical Hydrogels 3–24 (Elsevier, 2011). doi:10.1533/9780857091383.1.3.
- 18. Noshadi, I. et al. In vitro and in vivo analysis of visible light crosslinkable gelatin methacryloyl (GelMA) hydrogels. Biomater. Sci. 5, 2093–2105 (2017).
Descarga sugerida:
Artículo escrito por:
Helena Herrada-Manchón y Lucía Celada
Técnicos I+D+i, Unidad de Biofabricación, Departamento de Ingeniería de Procesos y Fabricación
Fundación IDONIAL, Gijón (Asturias).