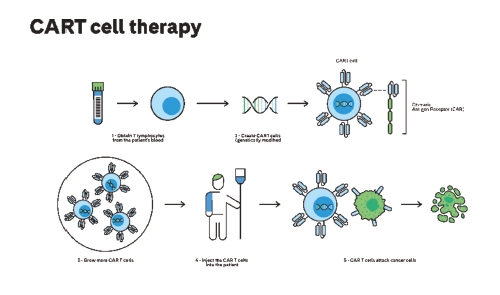
Las terapias CAR-T y las basadas en ARNm han transformado la medicina moderna, ofreciendo alternativas terapéuticas innovadoras para oncología, enfermedades raras y autoinmunes. Las CAR-T son una terapia nueva e innovadora para el tratamiento del cáncer en el que se utiliza al sistema inmune (linfocitos T autólogos modificados ex vivo) para reconocer y atacar las células tumorales específicas, mientras que las terapias de ARNm introducen instrucciones genéticas que permiten a las células producir proteínas terapéuticas transitorias.
Estas innovaciones plantean retos únicos en farmacovigilancia debido a la complejidad de sus mecanismos de acción, la aparición de efectos adversos graves y la necesidad de seguimiento prolongado.
La rápida aprobación de terapias de ARNm durante la pandemia de COVID-19 evidenció la necesidad de adaptar los sistemas regulatorios y de vigilancia post-comercialización. Por su parte, la biotecnología de las CAR-T introduce riesgos inmunológicos, neurológicos y hematológicos que requieren monitorización activa, registro riguroso y seguimiento a largo plazo.
Este artículo analiza los desafíos de la farmacovigilancia en terapias innovadoras, profundiza en los mecanismos de acción y propone estrategias para su integración efectiva en los sistemas de seguridad de medicamentos.
Mecanismos de acción y farmacovigilancia
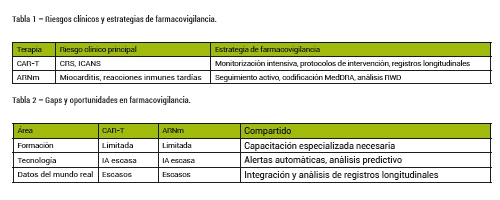
Las terapias CAR-T funcionan mediante la extracción de linfocitos T del paciente, los cuales se modifican genéticamente para expresar receptores quiméricos que reconocen antígenos tumorales específicos. Una vez reinfundidas, estas células se activan al identificar el objetivo, proliferan y destruyen las células malignas. Este mecanismo de acción, altamente efectivo, puede inducir efectos adversos graves, como el síndrome de liberación de citocinas (CRS) y la neurotoxicidad asociada a células efectoras inmunitarias (ICANS). Adicionalmente, pueden presentarse citopenias prolongadas, hipogammaglobulinemia e infecciones oportunistas, así como un riesgo teórico de inserción oncogénica. La farmacovigilancia en este contexto requiere una supervisión de la normativa proactiva, monitorización intensiva en tiempo real, protocolos de intervención inmediata, registro estandarizado de eventos, análisis longitudinal de los datos de los pacientes y medidas de reducción del riesgo.
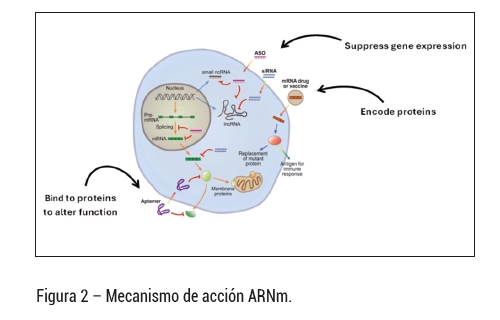
En paralelo, las terapias basadas en ARNm actúan introduciendo secuencias genéticas encapsuladas en nanopartículas lipídicas, que son absorbidas por las células para sintetizar proteínas terapéuticas transitorias. Estas proteínas pueden funcionar como antígenos en el caso de vacunas, o como proteínas funcionales terapéuticas. La activación del sistema inmune innato, la estimulación de receptores tipo Toll y la producción de interferones pueden causar inflamación sistémica y toxicidades tardías, incluyendo miocarditis y pericarditis. La farmacovigilancia de ARNm requiere seguimiento activo, codificación estandarizada de eventos mediante MedDRA y análisis de datos del mundo real para identificar efectos adversos poco frecuentes o tardíos.
Desafíos y brechas de la farmacovigilancia
A pesar de sus diferencias, las terapias CAR-T y ARNm comparten desafíos importantes para la farmacovigilancia:
- Poblaciones pequeñas de pacientes: Muchos ATMPs están indicados para condiciones raras o recidivantes, lo que limita los enfoques tradicionales de detección de señales.
- Perfiles de seguridad complejos y en evolución: por ejemplo, el CRS y el ICANS en la terapia CAR-T requieren un seguimiento de la seguridad en tiempo real y una formación especializada para los profesionales sanitarios. Además, los efectos adversos aún siguen identificándose.
- Seguimiento a largo plazo: necesario para las terapias de genes y ARN para controlar los acontecimientos adversos retardados, como la oncogenicidad.
- Modelos de tratamiento descentralizado: muchas terapias se administran en centros especializados, lo que complica el seguimiento y la notificación de eventos adversos.
- Sistemas de codificación inadecuados: las herramientas estándar, como MedDRA, pueden carecer de la especificidad necesaria para capturar nuevos acontecimientos adversos.
- Necesidad de nuevas metodologías PV: incluyendo registros de pacientes, Real World Evidence y análisis avanzados (por ejemplo, detección de señales basada en IA).
- Formación Especializada y Registros Longitudinales en PV: Los profesionales de farmacovigilancia deben contar con formación especializada y acceso a registros longitudinales que permitan evaluar riesgos de manera continua.
La modernización estructural y metodológica de la farmacovigilancia es esencial para garantizar la seguridad de los pacientes y la eficacia de estas terapias innovadoras sin frenar su desarrollo clínico.
A pesar de los avances actuales, siguen existiendo varias brechas críticas en el panorama actual de la farmacovigilancia, especialmente en el contexto de las terapias avanzadas e innovadoras:
- Falta de directrices específicas para las nuevas terapias. Aunque existen guías, la orientación sigue siendo limitada. Impacto: profesionales de PV deben interpretar la orientación general y tomar decisiones basadas en el riesgo con un precedente reglamentario limitado.
- Desafíos en la detección de señales y caracterización del riesgo. Las pequeñas poblaciones de pacientes y los eventos adversos inmunomediados raros hacen que los métodos tradicionales de detección de señales sean menos eficaces. Impacto: retrasos en la identificación de las señales de seguridad, lo que conduce a una mayor dependencia de los datos del mundo real y estrategias de vigilancia proactivas.
- Infraestructura de seguridad inadecuada a largo plazo. Las terapias genéticas y celulares requieren un seguimiento a largo plazo (hasta 15 años), pero los sistemas de recogida y gestión de estos datos suelen estar fragmentados o subdesarrollados. Impacto: Carga sobre los equipos de PV para diseñar planes personalizados de vigilancia a largo plazo y mantener la participación del paciente.
- Limitaciones en la integración de datos y pruebas en el mundo real (RWE). La falta de fuentes armonizadas de datos dificulta el uso eficiente de los RWE. Impacto: Los equipos de seguridad deben salvar las brechas de datos manualmente, ralentizando la toma de decisiones y aumentando las necesidades de recursos.
- Complejidad operativa. La administración descentralizada, las complejas cadenas de frío y la necesidad de centros especializados crean obstáculos logísticos para la presentación de informes sobre eventos adversos. Impacto: los líderes de PV deben establecer canales de comunicación sólidos con sitios, prescriptores y pacientes, a menudo fuera del ecosistema de informes estándar.
- Limitaciones de los recursos y déficit de talento. Las terapias avanzadas requieren una experiencia interdisciplinaria en materia de seguridad (clínica, normativa, ciencia de datos). Impacto: Aumento de la presión sobre los QPPV y los líderes fotovoltaicos para mejorar la cualificación de los equipos, gestionar la formación y garantizar el cumplimiento en nuevos escenarios.
Conclusiones
El futuro de la farmacovigilancia en terapias innovadoras depende de la capacidad de integrar sistemas digitales avanzados, colaboración internacional, análisis predictivo y evidencia del mundo real, además de una estrecha colaboración entre autoridades regulatorias, profesionales sanitarios y fabricantes. La modernización metodológica permitirá detectar riesgos emergentes de manera proactiva, garantizar la seguridad de los pacientes y acelerar la adopción segura de CAR-T y terapias de ARNm en la práctica clínica.
Agradecimientos
La autora agradece a Laura Fragata y Anam Ahmad del equipo de Vigilance de QbD por sus contribuciones en la elaboración de contenidos y análisis técnico.
Frases destacadas
La farmacovigilancia debe adaptarse a la complejidad y velocidad de desarrollo de terapias avanzadas.
Las terapias CAR-T y ARNm presentan perfiles de seguridad únicos que requieren vigilancia proactiva.
Lista de abreviaturas
- ARN: Ácido ribonucleico
- ARNm: ARN mensajero
- CAR-T: Células T con receptor quimérico de antígeno
- RAM: Reacción adversa a medicamentos
- EMA: Agencia Europea de Medicamentos
- FDA: Administración de Alimentos y Medicamentos
- CRS: Cytokine Release Syndrome
- ICANS: Immune effector Cell-Associated Neurotoxicity Syndrome
- MedDRA: Medical Dictionary for Regulatory Activities
- CIOMS: Council for International Organizations of Medical Sciences
- VEDRA: Veterinary Dictionary for Drug Regulatory Activities
- RWD: Real World Data
- PV: Farmacovigilancia
Descarga sugerida:
Artículo escrito por:
A. del Castillo
QBD, Global Head, Vigilance Division y Spain Country Manager
QbD