El ARN o ácido ribonucleico es una molécula que se compone de secuencias de nucleótidos unidos por enlaces fosfodiéster. Estos nucleótidos, a su vez, están compuestos por una base nitrogenada (púrica o pirimidínica) y un azúcar. En el ARN el azúcar es una ribosa y las bases nitrogenadas son: adenina (A), citosina (C), guanina (G) y uracilo (U), que sustituye a la timina (T) del ADN.
El ARN, por su composición, (más inestable que la del ADN) se encuentra en el núcleo de las células eucariotas así como en el citoplasma de las procariotas, pues constituye el único material genético que se produce para algunos virus. En los organismos celulares posee múltiples funciones: dirige las etapas intermedias de la síntesis proteica, regula la expresión génica y ejerce actividad catalítica, entre otras. Así, el ARN es mucho más versátil que el ADN (Figura 1).
En lo que respecta a su origen e historia, los ácidos nucleicos (ARN y ADN) fueron descubiertos en 1867 por Friedrich Miescher, médico suizo, que los llamó nucleína por aislarlos del núcleo celular de leucocitos y espermatozoides del salmón.? Posteriormente, se comprobó que las células procariotas, que carecen de núcleo, también contenían ácidos nucleicos. A finales del siglo XX, se pudo confirmar el papel del ARN en la síntesis de proteínas y veinte años después, Severo Ochoa ganaría el Premio Nobel de Medicina (1959), tras descubrir cómo se sintetizaba el ARN. En el año 2023 se corrobora la idea de que las moléculas de ARN fueron la primera forma de vida propiamente dicha en habitar el planeta Tierra (Hipótesis del mundo de ARN).
En lo que a clasificación y tipos existentes de ARN, el ARN mensajero (ARNm) es el ARN que lleva la información del ADN (desde el núcleo) a los ribosomas (citoplasma), para la síntesis de proteínas. De este modo, la secuencia de nucleótidos del ARNm determina la secuencia de aminoácidos de la proteína. Por este motivo al ARNm se le conoce también como ARN codificante (Figura 1). Sin embargo, muchos tipos de ARN no codifican proteínas, por lo que reciben el nombre de ARN no codificantes. Estos se originan a partir de genes propios (genes ARN) o son los intrones rechazados durante el proceso de empalme o ajuste. Un ejemplo de ARN no codificantes son el ARN de transferencia (ARNt) y el ARN ribosómico (ARNr), que son esenciales en el proceso de traducción, y diversos tipos de ARN reguladores (Figura 1).
Algunos ARN no codificantes (ribozimas) son capaces de catalizar reacciones químicas como cortar y unir otras moléculas de ARN o incluso formar enlaces peptídicos entre aminoácidos en el ribosoma durante la síntesis de proteínas.
Si nos centramos en su aplicabilidad, la flexibilidad y la celeridad en el desarrollo de terapias basadas en ARN ofrecen importantes ventajas en el tratamiento de enfermedades. La capacidad de adaptar las terapias para abordar mutaciones genéticas específicas representa un potencial único para hacer frente a las necesidades surgidas en el contexto de la medicina de precisión o personalizada. Desde su descubrimiento hasta las aplicaciones clínicas actuales, este campo dinámico está dando forma a un futuro donde las enfermedades sin tratamiento se pueden cronificar e incluso curar, lo que supone un nuevo paradigma en la medicina del futuro. La inmunización frente al coronavirus SARS-CoV-2 se ha realizado con vacunas basadas en ARN. Desde 2020, las enfermedades potencialmente candidatas a ser tratadas han ido aumentando paulatinamente: hereditarias (distrofias musculares o fibrosis quística) o adquiridas (cáncer, enfermedades infecciosas o enfermedades neurodegenerativas).
Un ejemplo concreto de terapia basada en ARN es Patisiran, un medicamento del laboratorio Alnylam (Estados Unidos) aprobado en 2018 tanto por la FDA como por la EMA. Este medicamento demostró ser efectivo frente a la amiloidosis, una enfermedad genética en la que versiones anormales de una proteína, transtiretina, se depositan en los tejidos, sobre todo en los nervios periféricos y en el corazón. Otra terapia basada en ARN es el medicamento Spinraza del laboratorio Biogen, aprobado en 2016 en Estados Unidos y en 2017 en Europa para el tratamiento de la atrofia muscular espinal, principal causa genética de muerte en neonatos.
A todo lo anterior, se suma el hecho de que el ARN puede emplearse como biomarcador, ya que ,tanto el ARNm como los ARN no codificantes, pueden utilizarse como indicadores de la actividad génica y celular, permitiendo valorar la progresión y pronóstico de una patología.
Si se profundiza en la indicación principal del medicamento y su intención de tratar, se observa que la amplia mayoría de terapias basadas en ARN (50%) están destinadas a hacer frente a infecciones virales, seguidas de las indicaciones oncológicas (30%) y por las indicaciones no oncológicas (trastornos respiratorios, metabólicos, neurológicos y cardiovasculares) que constituyen el 20%. Si se atiende a la evolución de ensayos clínicos anual destinados exclusivamente a este tipo de terapia, el resultado es aún más llamativo si cabe. El progreso en el número de ensayos ejecutados anualmente ha sido continuo, pero discreto y alza la última década, hasta 2020: momento en el que se pasó de menos de 5 ensayos clínicos/año (2011) a más de 20 (2020), lo que supone 4 veces más en solo 10 años. No obstante, estos datos resultan ínfimos si se consulta lo relativo al año 2021, que supuso un apogeo para las terapias basadas en ARNm alcanzando casi los 160 ensayos, cinco veces más en tan solo 1 año.
Este hecho no es casualidad ni aislado, pues sucedió en un contexto de pandemia, la COVID-19, lo que explicaría por qué el 90% de estos ensayos estaban centrados en el desarrollo de vacunas basadas en ARNm. Este hito supuso un antes y un después en lo que se refiere a las terapias basadas en ARN y todo lo que concierne a su investigación y regulación. Por todo lo descrito anteriormente, resulta imprescindible la correcta clasificación regulatoria de esta tipología de productos basados en ARN. De este modo, se debe comprender cuál es la definición de medicamento y si se trata de un medicamento de síntesis química, biológico o de terapia génica (GTMP), pues le aplicarán Directivas, normativas y partes de las Normas de Correcta Fabricación (NCF o GMP, de sus siglas en inglés) muy diferentes, lo que afecta a su ruta regulatoria y desarrollo.
Por definición, y siguiendo lo recogido en la Directiva 2001/83/CE, se entiende como medicamento de uso humano a “Toda sustancia o combinación de sustancias que se presente como poseedora de propiedades para el tratamiento o prevención de enfermedades en seres humanos o que pueda usarse en seres humanos o administrarse a seres humanos con el fin de restaurar, corregir o modificar las funciones fisiológicas ejerciendo una acción farmacológica, inmunológica o metabólica, o de establecer un diagnóstico médico”.
Asimismo, la Directiva 2001/83 define como un medicamento biológico a todo producto cuyo principio activo es biológico, siendo una sustancia activa biológica aquella que se produce o extrae a partir de una fuente biológica y que necesita, para su caracterización y determinación de su calidad, una combinación de ensayos fisicoquímicos y biológicos junto con el proceso de producción y su control.
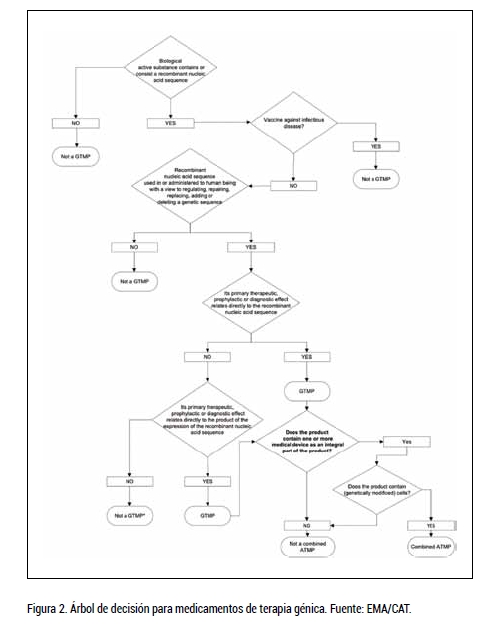
Si se habla de medicamento de terapia génica, es importante tener en cuenta lo recogido en la guía EMA/CAT/600280/2010 rev.1 y en la Directiva 2009/120/CE, siendo un medicamento de terapia génica un medicamento biológico que cumple con las dos siguientes características:
- “Incluye un principio activo que contiene un ácido nucleico recombinante, o está constituido por él, utilizado en seres humanos, o administrado a los mismos, con objeto de regular, reparar, sustituir, añadir o eliminar una secuencia génica.
- Su efecto terapéutico, profiláctico o diagnóstico depende directamente de la secuencia del ácido nucleico recombinante que contenga, o del producto de la expresión genética de dicha secuencia”.
En este sentido, se debe tener en cuenta que los medicamentos de terapia génica no incluyen las vacunas contra enfermedades infecciosas. Pues, por lo general, dichas vacunas presentan un efecto profiláctico en su modo de acción, mientras que si el producto tiene como objetivo el tratamiento de la enfermedad causada por la infección si podría ser considerado una terapia génica; tal y como queda recogido en la página 8 guía EMA/CAT/600280/2010 rev.1 Asimismo, se debe atender a que el ácido nucleico recombinante debe presentar un origen biológico independientemente del origen del vector utilizado (vectores virales, liposomas…).
No obstante, para asegurar una adecuada y rigurosa clasificación del producto, el Comité de Terapias Avanzadas (CAT) de la Agencia Europea del Medicamento (EMA) facilita el documento guía “Reflection paper on classification of advanced therapy medicinal products” que contiene el árbol de decisión para la clasificación regulatoria (Figura 2).
Bibliografía y normativa:
- Delaunay, S. et al. (2024). RNA modifications in physiology and disease: towards clinical applications. Nature reviews. Genetics, 25(2), 104–122. https://doi.org/10.1038/s41576-023-00645-2.
- Reflection paper on classification of advanced therapy medicinal products. EMA/CAT/600280/2010 rev.1. 21 May 2015.
- Reglamento (CE) No 1394/2007 del parlamento europeo y del consejo de 13 de noviembre de 2007 sobre medicamentos de terapia avanzada y por el que se modifican la Directiva 2001/83/CE y el Reglamento (CE) no 726/2004.
- Rovira, E. et al (2023). Engineering U1-Based Tetracycline-Inducible Riboswitches to Control Gene Expression in Mammals. ACS nano, 17(23), 23331–23346. https://doi.org/10.1021/acsnano.3c01994.
- Zhu, Y. et al. (2022). RNA-based therapeutics: an overview and prospectus. Cell Death Dis 13, 644 https://doi.org/10.1038/s41419-022-05075-2.
Descarga sugerida:
Artículo escrito por:
Javier Raboso Gallego
Responsable de I+D
Konexio Biotech